产品介绍:
GMP级无蛋白非程序细胞冻存液采用渗透性保护剂、非渗透性保护剂、细胞沉降稳定剂、细胞膜保护剂组合的方案对细胞进行全方位低温保护,可使冻存过程中溶液冰点降低,提高细胞膜对水的通透性,使细胞内水分在冻结前透出细胞,防止或减少冰晶对细胞的损伤,同时降低冰冻时细胞周围电解质浓度,避免电解质损伤,还可以延缓冻存过程中细胞的互相挤压,保护细胞膜,从而有效提高细胞复苏率和活力。
传统的细胞冻存液是使用培养基、血清和DMSO按照一定的比例混合,因其中的血清成分复杂、批次差异大等缺点,其应用具有局限性,且需要采用程序性降温的冻存方法,费时费力。GMP级无蛋白非程序细胞冻存液是一款Serum-Free、Animal Origin-Free、Protein-Free、Chemically Defined,不需要程序性降温的冻存液。与传统细胞冻存液相比具有明显优势(表1),冻存细胞复苏后的存活率也有明显提高(详情请见产品数据展示)。
GMP级无蛋白非程序细胞冻存液推荐用于各种常规哺乳动物细胞的冻存,尤其适合于无血清培养的干细胞、免疫细胞、蛋白表达细胞的冻存。
表1:传统细胞冻存液和GMP级无蛋白非程序细胞冻存液的特点比较
|
差异 |
传统细胞冻存液 |
GMP级无蛋白非程序细胞冻存液 |
|
血清 |
有 |
无 |
|
蛋白 |
有 |
无 |
|
成分是否明确 |
不明确 |
明确 |
|
程序降温 |
需要 |
不需要 |
|
冻存液配制 |
现用现配 |
即用型,无需配制,4℃保存,即取即用 |
|
内毒素 |
>0.5EU/ML |
<0.25EU/ML |
|
复苏存活率 |
一般(微量冻存时细胞存活率低) |
高(微量冻存时细胞存活率也高) |
|
批次差异 |
批次差异大 |
批次差异极小 |
|
整板冻存 |
不可行 |
可行,且方便快捷 |
|
安全性 |
有动物来源病毒、霉菌和支原体等污染风险 |
无动物来源病毒、霉菌和支原体等污染风险 |
|
申请药用辅料 |
极其困难 |
相对容易 |
|
能否用于临床 |
不可以,含动物血清、蛋白 |
可以,化学成分明确,无动物源成分,无蛋白 |
生产工艺:本产品使用注射用水(Water-For-Injection)配制,生产程序严格按照cGMP管理规定,并在体外诊断试剂备案净化车间中完成。 公司已取得ISO9001:ISO13485质量体系认证。
质控体系:GMP级冻存液,生产研发质控严格按照gmp标准执行,产品取得医疗器械备案,(备案号苏苏械备20210235),并进行了小鼠全身急毒实验,兔溶血性实验等临床毒理研究,表明本品安全可靠,CDE药用辅料登记进行中,可提供完整的工艺,质量,毒理研究数据,符合临床监管要求,纯化学成分,内毒素水平低于注射液国家标准,可以最大程度加快客户临床实验进程,欢迎联合申报。
产品优势:
Ø 安全——无血清,无动物源成分,无蛋白,化学成分明确。
Ø 高效——有效提高细胞复苏存活率,大部分细胞(包括间充质干细胞)复苏率可达90%以上。
Ø 稳定——不影响干细胞表型和生长状态,且可维持干细胞的多分化性。
Ø 便捷——即用型产品,且无需程序性降温,可直接-80℃过夜后转移至液氮中长期保存。
Ø 质优——严格的质量控制,产品性能媲美进口;原料均选用自产或者经过严格检测和纯化的低内毒素高纯药用级别原料;注射用水配置,符合GMP规定生产,工艺稳定,批差异小。进口材质无菌包装瓶,符合GMP管理规定,优秀的密闭性及内部涂层保护,极大的保证了产品的稳定性。
Ø 可靠——已有干细胞、免疫细胞、肿瘤和转化细胞系等多种细胞的冻存应用。
产品包装形式: 100ML每瓶。
保存条件:2~8℃保存。
运输条件:常温运输。
有效期:12个月。
产品数据展示:
1. 细胞复苏存活率
l GMP级无蛋白细胞冻存液组与进口C品牌无血清冻存液组在大部分细胞上存活率是相当的,在有些细胞上GMP级无蛋白细胞冻存液组的存活率更高(图1&2)。
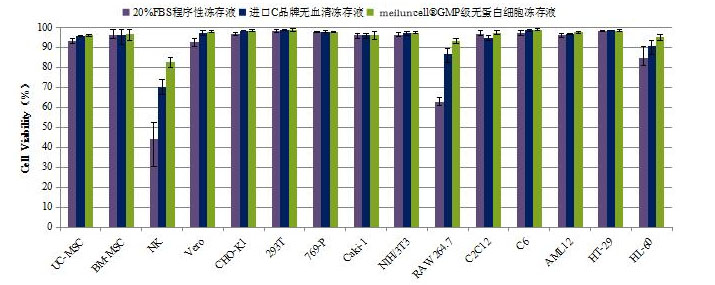 |
图1: 用GMP级无蛋白细胞冻存液、进口C品牌无血清冻存液、程序性冻存液(20%FBS+10%DMSO)在-80℃中冻存3-17天的多种细胞复苏后存活率比较。
 |
图2: 用GMP级无蛋白细胞冻存液、进口C品牌无血清冻存液、程序性冻存液(20%FBS+10%DMSO)在-80℃冻存3个月的多种细胞复苏后存活率比较。
2. 间充质干细胞复苏后贴壁情况
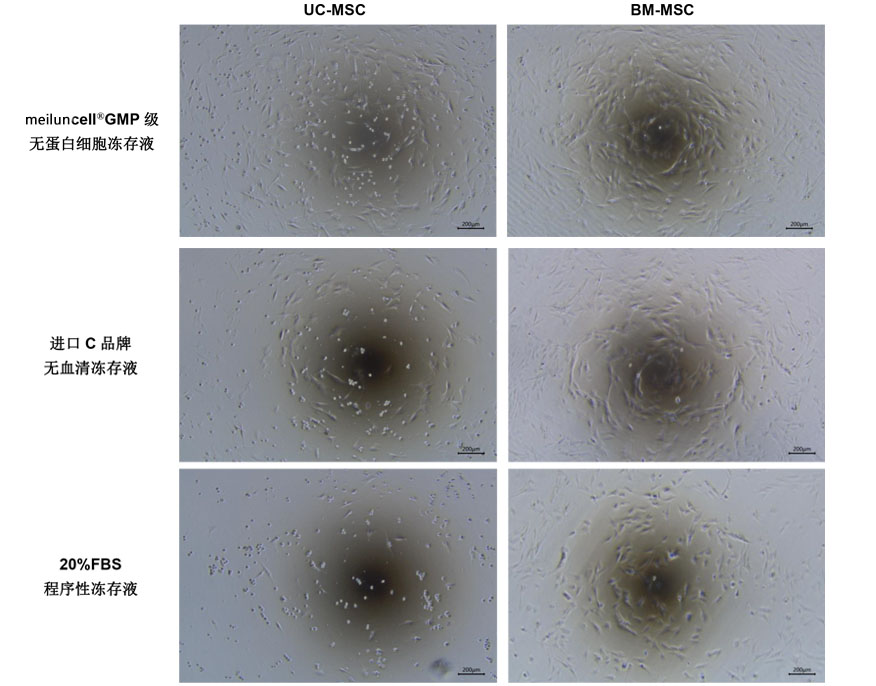
l 细胞复苏后将细胞数调整至1×10^5/ml,UC-MSC用无血清培养基培养,BM-MSC用DMEM-L+10%FBS培养,24h后换液并观察细胞贴壁情况。GMP级无蛋白细胞冻存液组比进口C品牌无血清冻存液组贴壁部分细胞更多(图3),冻存后不会影响间充质干细胞的贴附能力。
 |
|
图3: 用GMP级无蛋白细胞冻存液、进口C品牌无血清冻存液、程序性冻存液(20%FBS+10%DMSO)冻存间充质干细胞复苏后细胞贴壁情况的比较。
3. 细胞复苏后生长状态
l 细胞复苏后培养48h,观察生长情况。GMP级无蛋白细胞冻存液组与进口C品牌无血清冻存液组相比,细胞状态相当甚至更好(图4),冻存后不会影响间充质干细胞和其他贴壁细胞的生长。
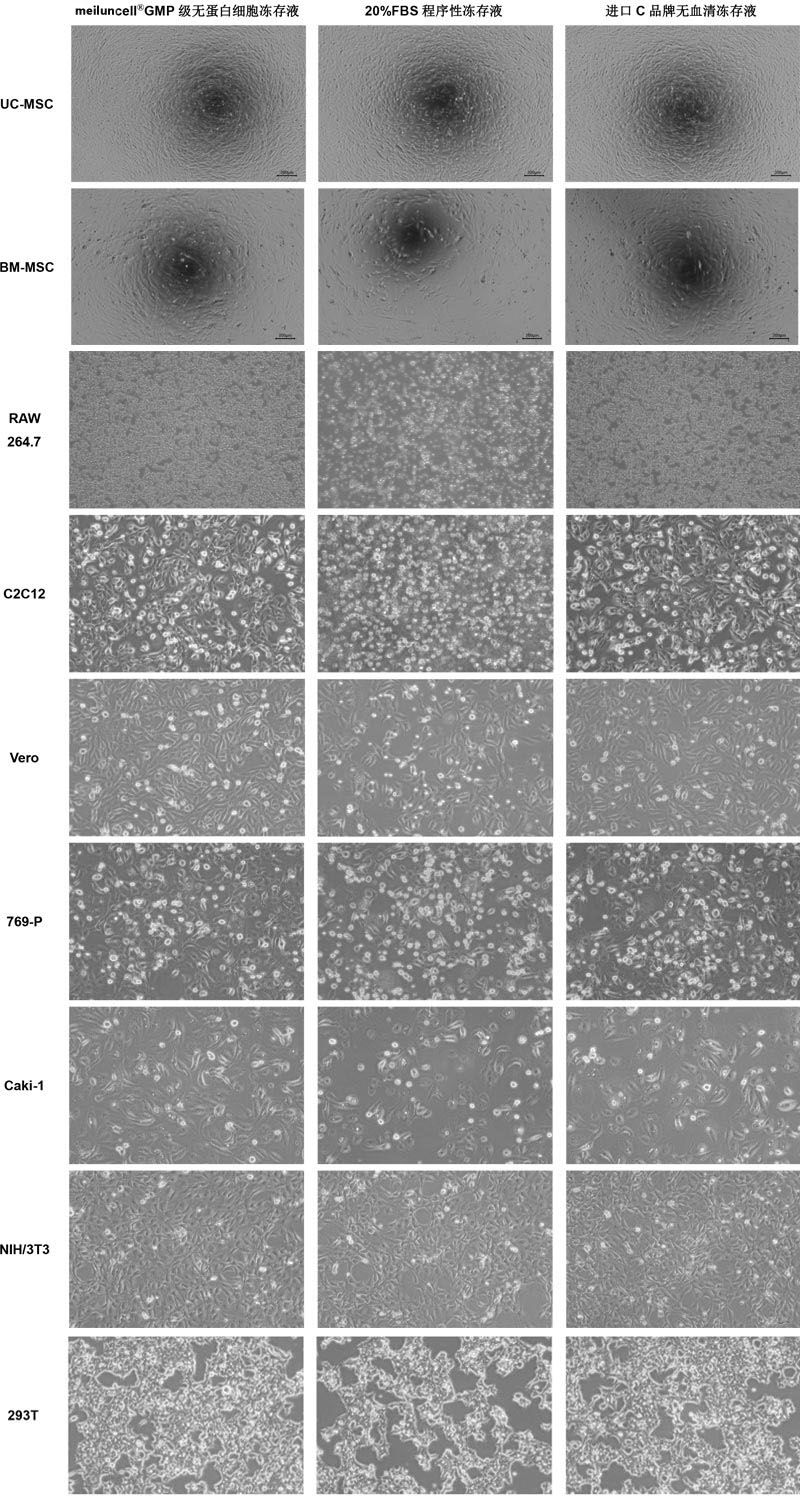
图4: 用GMP级无蛋白细胞冻存液、进口C品牌无血清冻存液、程序性冻存液(20%FBS+10%DMSO)冻存间充质干细胞和其他细胞系复苏后细胞生长状态的比较。
4. 对间充质干细胞标志物表达的影响
l 细胞复苏并传代两次后通过流式细胞术评估细胞标志物的表达。GMP级无蛋白细胞冻存液组能够维持CD105和CD90的阳性表达,和CD45阴性,没有观察到与程序性冻存液组标志物表达的差异(图5)。
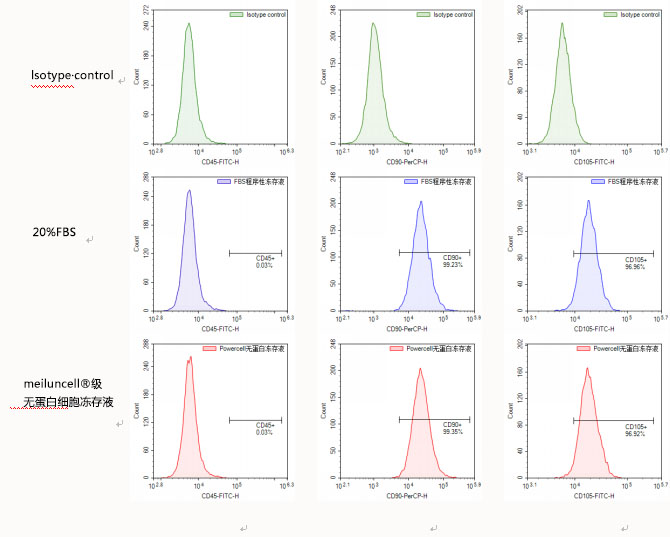
图5: 用GMP级无蛋白细胞冻存液、程序性冻存液(20%FBS+10%DMSO)冻存人脐带间充质干细胞复苏后细胞标志物的表达。
5. 对间充质干细胞分化潜能的影响
l GMP级无蛋白细胞冻存液冻存的细胞保留了三系分化潜能,成脂肪分化细胞形成可见的脂质空泡,呈现出典型的成脂分化;成骨分化细胞形成大量的钙结节,呈现典型的成骨分化;软骨细胞球体的切片和染色证明了硫酸软骨素和硫酸胶质等蛋白的存在,呈现典型的成软骨分化(图6)。

图6: 用GMP级无蛋白细胞冻存液冻存的人脐带间充质干细胞分化潜能的鉴定。将复苏后的MSC分化成(A)脂肪细胞、(B)骨细胞和(C)软骨细胞,分别用(A)油红O,(B)茜素红和(C)阿利新蓝进行染色。
英文名:GMP grade Protein-Free Cryopreservation Medium
质量标准:医疗级
| 质控指标 | 依据 | 标准 |
| 外观及澄清度 | 中华人民共和国药典2015版四部通则0901-0902 | 无可见异物,淡黄色透明液体 |
| pH值 | 中华人民共和国药典2015版四部通则0631 | 6.9~7.2 |
| 渗透压 | 中华人民共和国药典2015版四部通则0632 | 1900~2300 mOsm/kgH2O |
| 细菌内毒素 | 中华人民共和国药典2015版四部通则1143 | <0.25 EU/ml |
| 微生物检测 | 中华人民共和国药典2015版四部通则1101 | 无菌 |
| 支原体 | 中华人民共和国药典2015版四部通则3301 | 阴性 |
| 细胞冻存效果 | 内部SOP | 细胞复苏率高于对照 |
